Экспресс-анализ проб мочи методом масс-спектрометрии с ионизацией, индуцированной лазерной плазмой при атмосферном давлении
Аннотация
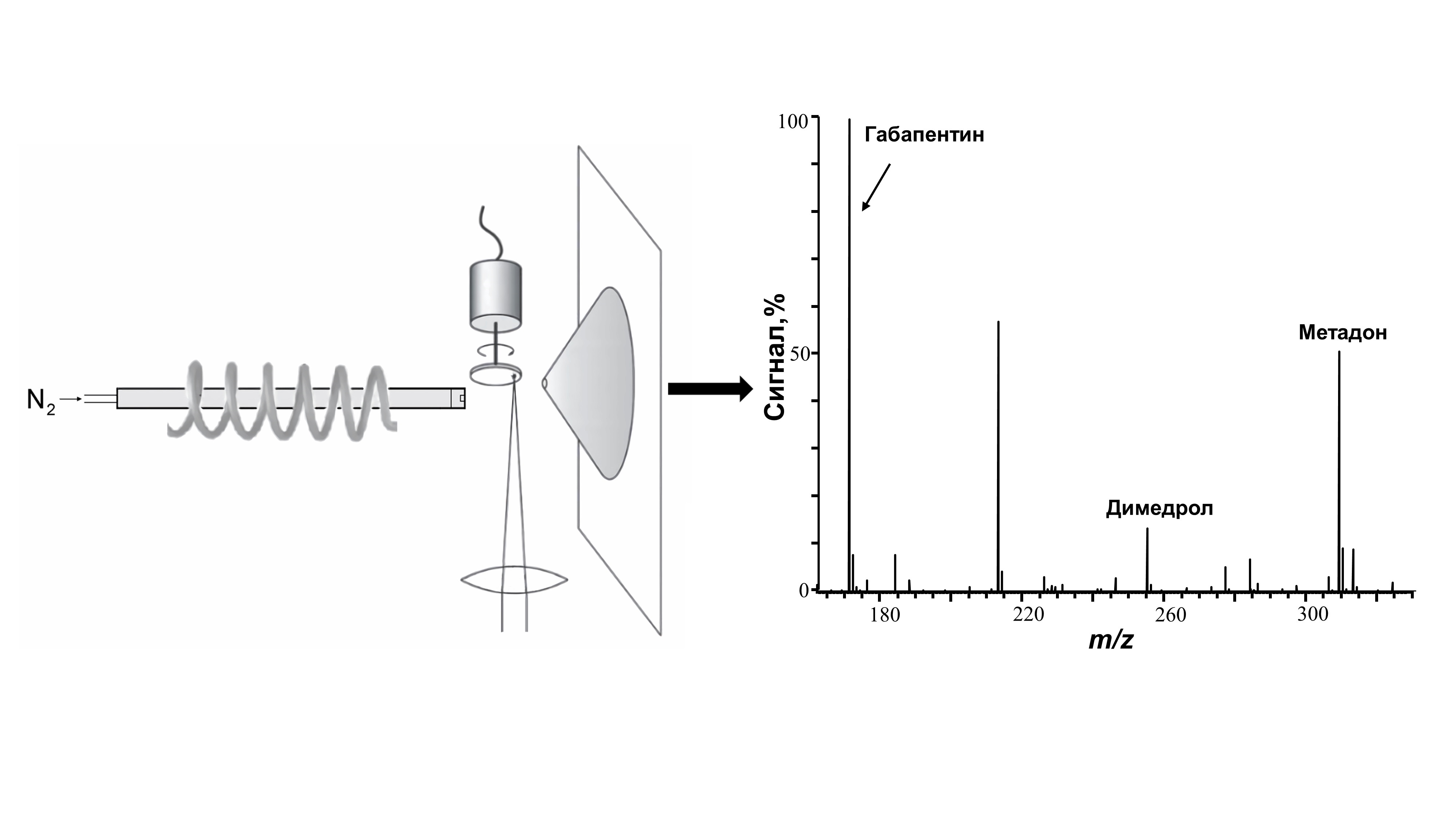
APLPI), исследован для решения проблемы быстрого определения физиологически активных веществ
в моче. Задачи исследования включали: изучение методом APLPI образцов мочи, полученных от
проходящих лечение пациентов; определение аналитических характеристик метода; сравнительные
исследования методов APLPI и ВЭЖХ-МС/МС по отношениям сигнал/шум и оценка возможности
скрининга образцов мочи без пробоподготовки методом APLPI.
Приборная реализация метода основана на использовании масс-анализатора высокого
разрешения “Orbitrap”, в котором штатный ионный источник заменен на разработанный нами
источник APLPI, в сочетании с термодесорбционным вводом пробы. Исследовали образцы мочи, в
которых предварительно методом ВЭЖХ-МС/МС обнаружены физиологически активные вещества,
в частности, барбитураты, карбамазепин, тиаприд, сульпирид, псилоцин, амфетамин, трамадол,
димедрол и другие. Установлено, что метод APLPI обеспечивает возможность детектирования всех
этих аналитов. Длительность анализа одной пробы не превышает одну минуту.
С использованием способа «разбавление в матрице» построили градуировочные зависимости
для ряда соединений и определили аналитические характеристики метода. Градуировочные
зависимости линейны в диапазоне трех порядков величины. Среднее значение относительного
стандартного отклонения ионного сигнала в этом диапазоне составило 24 %. Пределы обнаружения,
найденные на примере определения димедрола, лидокаина и фенобарбитала в экстрактах мочи
составили 0.7 нг/мл, 0.5 нг/мл и 10 нг/мл, соответственно. Сравнительные исследования показали,
что методы APLPI и ВЭЖХ-МС/МС характеризуются близкими значениями отношений сигнал/шум.
Преимущества метода APLPI заключаются в экспрессности, ретроспективности анализа, в малом
объеме проб. Ограничением метода является необходимость десорбции определяемых соединений
в газовую фазу. Продемонстрирована возможность применения метода APLPI для скрининга
физиологически активных веществ в моче без предварительной пробоподготовки.
Ключевые слова: масс-спектрометрия с ионизацией при атмосферном давлении, лазер-
но-индуцированная плазма, скрининг лекарственных соединений в моче.
Полный текст:
PDFЛитература
REFERENCES
Lebedev A. T. Mass-spektrometriya v organicheskoj himii [Mass spectrometry in organic chemistry]. Moscow, Tekhnosfera Publ, 2015. 704 p. (in Russian).
Foltz R.L, Fentiman A.F., Foltz R.B. GC/MS assays for abused drugs and body fluids. National Institute on Drug Abuse Research Monograph Series 32. Rockville, Maryland, 1980. 202 p.
Virus E.D., Ivanov A.V., Luzyanin B.P., Kubatiev A.A. [Review. Mass spectrometry of physiologically active substances prohibited in sports: the problem of screening a wide range of compounds and their metabolites]. Mass-spektrometriya [Mass Spectrometry], 2017, vol. 14, no. 3, pp. 54-57 (in Russian).
Thevis M., Kuuranne T., Geyera H., Schänzera W. Annual banned-substance review: analytical approaches in human sports drug testing // Drug Test. Anal., 2017, vol. 9, pp. 6–29. doi 10.1002/dta.2139.
Wright T., Harris C. Twenty-one cases involving alpha- pyrrolidinovalerophenone (α-PVP) // J. Anal. Toxiс., 2016, vol. 40, pp. 396–402. doi: 10.1093/jat/bkw029.
Maurer H. Pitfalls in drug testing by hyphenated low- and high-resolution mass spectrometry // Drug Test Anal., 2020, vol. 12, pp. 172–179. doi: 10.1002/dta.2744.
Guale F., Shahreza S., Walterscheid J., Chen H., Arndt C., Kelly A., Mozayani A. Validation of LC–TOF-MS screening for drugs, metabolites, and collateral compounds in forensic toxicology specimens // J. Anal. Toxic., 2012, vol. 00, pp. 1–8. doi:10.1093/jat/bks084.
Strickland E., Cummings O., Mellinger A., McIntire G. Development and validation of a novel all-inclusive LC–MS-MS designer drug method // J. Anal. Toxic., 2019, vol. 43, pp. 161–169. doi: 10.1093/jat/bky087.
Maurer H.H., Pfleger K., Weber A.A. Mass spectral and GC data of drugs, poisons, pesticides, pollutants, and their metabolites, 5th Edition. German, 2016. 1756 p.
Lin D.L., Wang S.M., Wu C.H., Chen B.G., and Liu R.H. Chemical derivatization for the analysis of drugs by GC-MS - a conceptual review. // J. Food Drug Anal., 2008, vol. 16, no. 1, Article 1. doi: 10.38212/2224-6614.2373
Thevis M., Thomas A., Pop V., Schänzer W. Ultrahigh pressure liquid chromatography-(tandem) mass spectrometry in human sports drug testing: possibilities and limitations // J. Chromatogr. A, 2013, vol. 31, no. 1292, pp. 38–50. doi: 10.1016/j.chroma.2012.12.048.
Peters F.T. Recent advances of liquid chromatography–(tandem) mass spectrometry in clinical and forensic toxicology // Clin. Biochem., 2011, vol. 44, no. 1. pp. 54–65. doi: 10.1016/j.clinbiochem.2010.08.008.
Pento, A.V., Nikiforov, S.M., Simanovsky, Y.O., Grechnikov, A.A., Alimpiev, S.S. Laser ablation and ionisation by laser plasma radiation in the atmospheric-pressure mass spectrometry of organic compounds // Quantum Electron. 2013, vol. 43, no. 1, pp. 55-59. doi: 10.1070/QE2013v043n01ABEH015065.
Bierstedt A., Riedel J. Airborne laser-spark for ambient desorption/ionization // Eur. J. Mass Spectrom, 2016, vol. 22, no. 3, pp. 105-114. doi: 10.1255/ejms.1417.
Kravets K.Yu., Grechnikov A.A., Simanovsky Ya.O. [Ionization of organic compounds affected by laser plasma radiation at atmospheric pressure] // J. Analyt. Chem, 2021, vol. 76, no. 14, pp. 217-224. doi: 10.25703/MS.2020.39.25.001.
Pento A.V., Bukharina A.B., Nikiforov S.M., Simanovsky Y.O., Sartakov B.G., Ablizen R.S., Fabelinsky V.I., Smirnov V.V., Grechnikov A.A. Laser-induced plasma on a metal surface for ionization of organic compounds at atmospheric pressure // Int. J. Mass Spectrom., 2021, vol. 461, Artical 116498. doi: 10.1016/j.ijms.2020.116498.
Kravets K.Yu, Timakova S.I., Grechnikov A.A., Borodkov A.S., Laptinskaya P.K., Kuzmin V.S., Simanovsky Ya O. [Screening of medicinal compounds in blood by atmospheric pressure laser plasma ionization mass spectrometry] // J. Analyt. Chem., 2022, vol. 77, no. 1, pp. 1307-1314. doi: 10.1134/S1061934822100082.
Kim S., Rodgers R.P., Marshall A.G. Truly «exact» mass: Elemental composition can be determined uniquely from molecular mass measurement at similar to 0.1 mDa accuracy for molecules up to similar to 500 Da // Int. J. Mass Spectrom., 2006, vol. 251, no. 2–3, pp. 260–265. doi: 10.1016/j.ijms.2006.02.001.
Makarov A. Practical aspects of ion trap mass spectrometry. Volume IV: Theory and Instrumentation. U.S.: CRC Press (Taylor & Francis). 2009. 922 p.
Makarov A., Denisov E., Kholomeev A., Balschun W., Lange O., Strupat K. & Horning S. Performance evaluation of a hybrid linear ion trap/orbitrap mass spectrometer // Anal. Chem., 2006, vol. 78, no. 7, pp. 2113-2120. doi: 10.1021/ac0518811.
DOI: https://doi.org/10.15826/analitika.2023.27.3.002
Ссылки
- На текущий момент ссылки отсутствуют.
