ОПРЕДЕЛЕНИЕ ХИНИНА В БЕЗАЛКОГОЛЬНЫХ НАПИТКАХ МЕТОДОМ ФЛУОРИМЕТРИИ
Аннотация
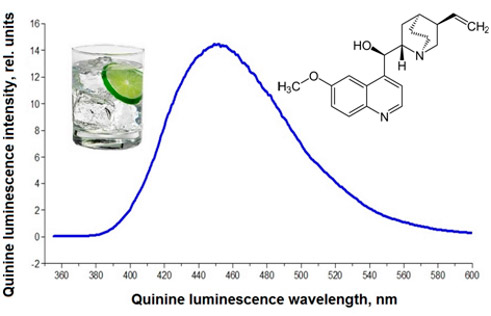
Флуориметрический метод предложен для качественного и количественного определения пищевой вкусоароматической добавки хинина в напитках-тониках. Выбор данного метода обусловлен его высокой чувствительностью, селективностью и экспрессностью по сравнению с другими методами. Найдены оптимальные условия флуориметрического определения хинина в напитках: растворитель – 0.01 М серная кислота, длина волны возбуждения 353 нм, длина волны люминесценции 452 нм, параметры строба – задержка сигнала 0.85 мкс, длительность сигнала 21.25 мкс. Для увеличения чувствительности разрабатываемой методики проведены исследования люминесценции хинина и определены квантовые выходы люминесценции хинина в различных концентрациях серной кислоты от 0.005 до 1.000 М. Установлено, что наибольшая интенсивность люминесценции хинина, наибольший квантовый выход и наименьший сигнал фона растворителя наблюдается в 0.01 М H2SO4. Исследовано влияние мешающих компонентов пищевой матрицы на флуориметрическое определение хинина. Установлено, что сахар и лимонная кислота не влияют на люминесцентный сигнал хинина. Рассчитан предел обнаружения хинина, который составил 0.0019 мг/дм3. Для проверки правильности флуориметрической методики проведено сравнение результатов со спектрофотометрической методикой определения хинина в напитках (максимальное поглощение хинина при 347 нм). Результаты, полученные двумя методиками, хорошо согласуются, при этом предел обнаружения флуориметрического метода ниже по сравнению с известными методами. Предложенная методика может быть использована для контроля качества и безопасности безалкогольных напитков.
Ключевые слова: хинин, флуориметрия, напитки-тоники, квантовый выход люминесценции, параметры строба
Полный текст:
PDF (Russian)Литература
REFERENCES
Samanidou V.F., Evaggelopoulou E.N., Papadoyannis I. N. Simple and Rapid HPLC Method for the Determination of Quinine in Soft Drinks Using Fluorescence Detection. J. of Liquid Chrom. & Rel. Technol., 2004, vol. 27, no. 15, pp. 2397-2406. doi:10.1081/jlc-200028156.
Donovan J.L., De Vane C.L., Boulton D., Dodd S., Markowitz J. S. Dietary levels of quinine in tonic water do not inhibit CYP2D6 in vivo. Food and Chemical Toxicology, 2003, vol. 41, no. 8, pp. 1199-1201. doi:10.1016/s0278-6915(03)00112-1.
Sanitarno-epidemiologicheskie pravila i normativy "SanPiN 2.3.2.1078-01" ot 22.03.2002 g. [Sanitary and epidemiological rules and regulations "SanPiN 2.3.2.1078-01" dated March 22, 2002] (in Russian).
Chen Q.C., Wang J. Determination of quinine in drink by reversed-phase ion-pair chromatography. J. Liq. Chromatogr. Relat. Techno.l, 2001, vol. 24, no. 9, pp. 1341-1352.
Chmurzynski L. High-performance liquid chromatographic determination of quinine in rat biological fluids. J. Chromatogr. B: Biomed. Appl., 1997, vol. 693, no. 2, pp. 423-429.
Kluska M., Marciniuk-Kluska A., Prukała D., Prukała W. Analytics of Quinine and its Derivatives. Critical Reviews in Analytical Chemistr, 2015, vol. 46, no. 2, pp. 139-145. doi:10.1080/10408347.2014.996700.
Mustafa A.M., Ricciutelli M., Maggi F., Sagratini G., Vittori S., Caprioli G. Simultaneous Determination of 18 Bioactive Compounds in Italian Bitter Liqueurs by Reversed-Phase High-Performance Liquid Chromatography–Diode Array Detection. Food Analytical Methods, 2013, vol. 7, no. 3, pp. 697-705. doi: 10.1007/s12161-013-9727-0.
Reijenga J.C., Aben G.V.A., Lemmens A.A.G., Verheggen T.P.E.M., De Bruijn C.H.M.M., Everaerts F.M. Determination of quinine in beverages, pharmaceutical preparations and urine by isotachophoresis. Journal of Chromatography A. 1985, vol. 320, no. 1, pp. 245-252. doi:10.1016/s0021-9673(01)90502-3.
Xu L., Zhao W., Chang R., Zhang G., Zhang H., Chen A. Separation and determination of cinchona alkaloids by ligand-exchange capillary electrophoresis using a Cu(II)–l-lysine complex as selector. Journal of the Iranian Chemical Society, 2018. vol. 15, no. 7, pp. 1477-1483. doi:10.1007/s13738-018-1345-8.
Zhao W., Li Y., Zhang Y., Zhang H., Yu H., Chen A. Determination of Cinchona Alkaloids by Capillary Electrophoresis with Novel Complex Formation. Analytical Letters, 2015, vol. 49, no. 8, pp. 1176-1183. doi:10.1080/00032719.2015.1089258.
Dar R. A., Brahman P. K., Tiwari S., Pitre K. S. Electrochemical studies of quinine in surfactant media using hanging mercury drop electrode: A cyclic voltammetric study. Colloids and Surfaces B: Biointerfaces, 2012, vol. 98, pp. 72-79. doi:10.1016/j.colsurfb.2012.04.035.
Buleandra M., Rabinca A.A., Cheregi M.C., Ciucu A.A. Rapid voltammetric method for quinine determination in soft drinks. Food Chemistry, 2018, vol. 253, pp. 1-4. doi:10.1016/j.foodchem.2018.01.130
Kudláček K., Nesměrák K., Štícha M., Kozlík P., Babica J. Historical injection solutions of quinine analyzed by HPLC/MS. Monatshefte Für Chemie - Chemical Monthly, 2017, vol. 148, no. 9, pp. 1613-1618. doi:10.1007/s00706-017-1940-x
Feás X., Fente C.A., Cepeda A. Fast and Sensitive New High Performance Liquid Chromatography Laser Induced Fluorescence (HPLC-LIF) Method for Quinine. Comparative Study in Soft Drinks. Journal of Liquid Chromatography & Related Technologies, 2009, vol. 32, no. 17, pp. 2600-2614. doi:10.1080/1082607090324.
Mikuš P., Maráková K., Veizerová L., Piešt’anský J. Determination of quinine in beverages by online coupling capillary isotachophoresis to capillary zone electrophoresis with UV spectrophotometric detection. Journal of Separation Science, 2011, vol. 34, no. 23, pp. 3392-3398. doi:10.1002/jssc.201100633.
Lawson-Wood K., Evans K. Determination of Quinine in Tonic Water Using Fluorescence Spectroscopy. Available at: https://www.perkinelmer.com/lab-solutions/resources/docs/APP_Quinine_in_Tonic_Water_014133_01.pdf (accessed 15 June 2019).
O’Reilly J. E. Fluorescence experiments with quinine. Journal of Chemical Education, 1975, vol. 52, no. 9, pp. 610-612. doi:10.1021/ed052p610.
Infante C.M.C., Masini J. C. Development of a fluorimetric sequential injection analysis (SIA) methodology for determination of quinine. Journal of the Brazilian Chemical Society, 2011, vol. 22, no. 10. pp. 1888-1893. doi:10.1590/s0103-50532011001000009.
Metelica S.I., Kireeva E.V., Nemihin V.V., Kachin S.V., Losev V.N., Sagalakov S.A. [Extraction-fluorimetric determination of codeine in human urine] // Analitika i kontrol' [Analytics and control], 2017, vol. 21, no. 4, pp. 315-321 (in Russian). doi:10.15826/analitika.2017.21.4.006
Boulebd H., Ismaili L., Khatyr A., May A., Belfaitah A. New highly fluorescent hybrids (benz)imidazol-2-aminonicotinonitrile and -2-aminoisophthalonitrile: synthesis, characterization, fluorescence study, and theoretical calculations. Monatshefte Für Chemie - Chemical Monthly, 2018, vol. 149, no. 6, pp. 1125-1136.doi:10.1007/s00706-018-2141-y.
Shvaykova M.D. Toksikologicheskaya khimiia [Toxicological chemistry]. M.: Medicine 1975. 376 p. (in Russian).
Levin A.D., Nagaev A.I., Sadagov A.Ju., Karahotin S.N. [Qualitative analysis of wines based on the joint use of their optical spectra of different physical nature] Analitika i kontrol' [Analytics and control], 2018, vol. 22, no. 2, pp.147-156. doi: 10.15826/analitika.2018.22.2.001
D. Parker. Fotoliuminestsentsiia rastvorov [Photoluminescence of solutions]. Moscow, Mir Publ., 1972. (in Russian).
Kulakova I.I., Fjodorova O.A., Horoshutina A.V. Metody opticheskoi spektroskopii [Optical spectroscopy methods] Moscow, MSU M.V. Lomonosov, 2015.
Pacaeva S.V., Juzhakov V.I. Spetspraktikum kafedry obshchej fiziki «Elektronnye spektry slozhnykh molekul» [Special practical work of the department of general physics "Electronic spectrum of complex molecules"], Moscow, MSU M.V. Lomonosov, 2010.
Belikov V.G. Farmatsevticheskaia khimiia [Pharmaceutical Chemistry]. Part 2. Pyatigorsk 1996. 608 p. (in Russian
Ссылки
- На текущий момент ссылки отсутствуют.
