ОПРЕДЕЛЕНИЕ КОФЕИНА В НАПИТКАХ МЕТОДОМ ВОЛЬТАМПМЕРОМЕТРИИ НА УГЛЕРОДСОДЕРЖАЩИХ ЭЛЕКТРОДАХ, МОДИФИЦИРОВАННЫХ АРИЛДИАЗОНИЕВЫМИ СОЛЯМИ
Аннотация
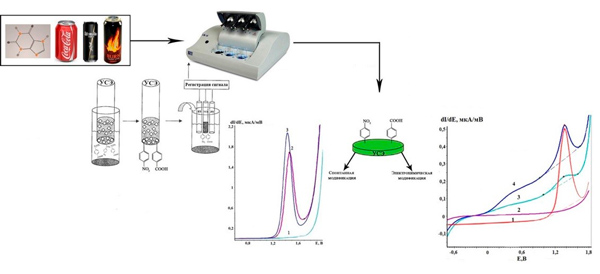
Предложен способ модификации углеродсодержащих электродов (УСЭ) тозилатными солями арендиазония (АДТ) с нитро- и карбоксизаместителями для вольтамперометрического (ВА) определения кофеина в напитках. Впервые проведено сравнение спонтанного химического и электрохимического способов модификации УСЭ АДТ для ВА определения кофеина. Новый класс АДТ обладает хорошей растворимостью, стабильностью в течение одного месяца, что играет немаловажную роль в процессе модификации поверхностей электродов. Подобраны оптимальные условия спонтанной химической модификации УСЭ: модификатор АДТ с NO2-заместителем, время погружения электрода в раствор модификатора − 10 с, концентрация модификатора − 5 мг/дм3. Методами инфракрасной спектроскопии (ИК-спектроскопии) и сканирующей электронной микроскопии (СЭМ) подтверждено закрепление АДТ на поверхности УСЭ с образованием ковалентных связей между атомами углерода электродной поверхности и бензольными кольцами модификатора. Показано, что после модификации площадь электроактивной поверхности увеличивается в два раза. В результате этого наблюдается возрастание чувствительности определения кофеина с пределом обнаружения 51 мг/дм3 и расширение диапазона определяемых концентраций: 154-500 мг/дм3. При использовании модифицированного электрода время анализа сократилось до 15 минут. Кроме этого, наблюдалась стабильность поверхности электрода без обновления в течение недели. При апробации пригодности для аналитических целей УСЭ, модифицированного АДТ с NO2-заместителем, проведено определение кофеина в некоторых тонизирующих и газированных напитках. Полученные значения содержания кофеина в напитках разработанным методом с использованием УСЭ, модифицированного спонтанным химическим способом АДТ с NO2-заместителем, наглядно демонстрируют соответствие значениям, заявленным производителем, а также согласуются с результатами независимого спектрофотометрического метода.
Ключевые слова: кофеин, ароматические соли диазония, модификатор, углеродсодержащий электрод, вольтамперометрия, спонтанная модификация, СЭМ, ИК-спектроскопия, циклическая вольтамперометрия
Полный текст:
PDF (Russian)Литература
REFERENCES
Cauli O., Morelli M. Caffeine and the dopaminergic system. Behav. Pharmacol., 2005, vol. 16, no. 2, pp. 63-77. doi: 10.1097/00008877-200503000-00001.
Heaney R. P. Effects of caffeine on bone and the calcium economy. Food Chem. Toxicol., 2002, vol. 40, no. 9, pp.1263-1270. doi: 10.1016/S0278-6915(02)00094-7.
Knight C. A., Knight I., Mitchell D. C. and Zepp J. E. Beverage caffeine intake in US consumers and subpopulations of interest: estimates from the Share of Intake Panel survey. Food Chem. Toxicol., 2004, vol. 42, no. 12, pp. 1923-1930. doi: 10.1016/j.fct.2004.05.002.
Hillel B., Hugh C. Rapid Analysis of Caffeinated Energy Drinks by HPLC on Ascentis Express, Reporter US. 2011. vol. 28.4, pp. 1-4.
Bhawani S. A., Fong S. S., Ibrahim M. N. Spectrophotometric Analysis of Caffeine. International J. Anal. Chem., vol. 2015, Article ID 170239, pp. 1-7. doi: 10.1155/2015/170239.
Emre D., Ozaltin N. Simultaneous determination of paracetamol, caffeine andpropyphenazone in ternary mixtures by micellar electrokinetic capillary chro-matography. J. Chromatogr. B, 2007, vol. 847, no. 2, pp. 126-132. doi: 10.1016/j.jchromb.2006.09.036.
Oren T., Anik U. Carboxylic acid functionalized multi-walled carbon nanotubes assisted centri-voltammetry as a new approach for caffeine detection. New J. Chem., 2013, vol. 41, no. 20, pp. 11800-11806. doi: 10.1039/c7nj02506h.
Kutonova K.V., Trusova M. E., Postnikov P. S., Filimonov V. D., Parello J. A simple and effective synthesis of aryl azides via arenediazonium tosylates. Synthesis, 2013, vol. 45, no. 19, pp. 2706-2710. doi: 10.1055/s-0033-1339648.
Molaakbari E., Mostafavi A., Beitollahic H., Simultaneous electrochemical determination of dopamine, melatonin, methionine and caffeine. Sens. Actuators, B, 2015, vol. 208, pp. 195-203. doi: 10.1016/j.snb.2014.10.130.
Fernandes D. M., Silva N., Pereira C. et al. MnFe2O4@CNT-N as novel electrochemical nanosensor for determination of caffeine, acetaminophen and ascorbic acid. Sens. Actuators B, 2015, vol. 218, pp. 128-136. doi: 10.1016/j.snb.2015.05.003.
Yiğita A., Yardıma Y., Çelebib M., Leventc A., Şentürkd Z. Graphene / Nafion composite film modified glassy carbon electrode for simultaneous determination of paracetamol, aspirin and caffeine in pharmaceutical formulations. Talanta, 2016, vol. 158, pp. 21-29. doi: 10.1016/j.talanta.2016.05.046.
Hernandez-Aldave S., Tarat A., McGettrick J. D., Bertoncello P. Voltammetric detection of caffeine in beverages at nafion / graphite nanoplatelets layer-by-layer films. Nanomaterials, 2019, vol. 9, no. 221, pp. 1-20. doi:10.3390/nano9020221
Farag A. S., Pravcová K., Česlová L., Vytřas K., Sýs M. Simultaneous determination of caffeine and pyridoxinein energy drinks using differential pulse voltammetryat glassy carbon electrode modified with nafion. Electroanalysis, 2019, vol. 31, pp. 1-7. doi: 10.1002/elan.201800646.
Tyszczuk-Rotko K., Pietrzak K., Sasal A. Adsorptive stripping voltammetric method for the determination of caffeine at integrated three-electrode screen-printed sensor with carbon / carbon nanofibers working electrode. Adsorption, 2019, vol. 25, pp. 913-921. doi: 10.1007/s10450-019-00116-3.
Tyszczuk-Rotko K., Szwagierek A. Green electrochemical sensor for caffeine determination in environmental water samples: the bismuth film screen-printed carbon electrode. J. Electrochem. Soc., 2017, vol. 164, no. 7, pp. 342-348. doi: 10.1149/2.0571707jes.
Tefera M., Geto A., Tessema M., Admassie S. Simultaneous determination of caffeine and paracetamol by square wave voltammetry at poly (4-amino-3-hydroxynaphthalene sulfonic acid)-modified glassy carbon electrode. Food Chem., 2016, vol 210, pp. 156-162. doi: 10.1016/j.foodchem.2016.04.106.
Mahanthappa M., Yellappa S., Kottam N., Rao Vusa C.S. Sensitive determination of caffeine by copper sulphide nanoparticlesmodified carbon paste electrode. Sens. Actuators, A, 2016, vol. 248, pp. 104-113. doi: 10.1016/j.sna.2016.07.013.
Chitravathi S., Munichandraiah N. Voltammetric determination of paracetamol, tramadol and caffeine using poly (Nile blue) modified glassy carbon electrode. J. Electroanal. Chem., 2016, vol. 764, pp. 93-103. doi: 10.1016/j.jelechem.2016.01.021.
Wang Y., Wu T., Bi C-Y. Simultaneous determination of acetaminophen, theophylline and caffeine using a glassy carbon disk electrode modified with a composite consisting of poly (Alizarin Violet 3B), multiwalled carbon nanotubes and graphene. Microchim Acta, 2016, vol.183, pp. 731-739. doi: 10.1007/s00604-015-1688-0.
ÖrenT., Anık Ü. Voltammetric determination of caffeine by using gold nanoparticle-glassy carbon paste composite electrode. Measurement, 2017, vol. 106, pp. 26-30. doi: 10.1016/j.measurement.2017.04.031.
Trani A., Petrucci R., Marrosu G., Zane D., Curulli A. Selective electrochemical determination of caffeine at a gold-chitosan nanocomposite sensor: May little change on nanocomposites synthesis affect selectivity. J. Electroanal. Chem., 2017, vol. 788, pp. 99-106. doi: 10.1016/j.jelechem.2017.01.049.
Mekassa B., Tessema M., Chandravanshi B. S. Simultaneous determination of caffeine and theophylline using square wave voltammetry at poly (L-aspartic acid) / functionalized multi-walled carbon nanotubes composite modified electrode. Sensing and Bio-Sensing Research, 2017, vol. 16, pp. 46-54. doi: 10.1016/j.sbsr.2017.11.002.
Amare M., Aklog S. Electrochemical determination of caffeine content in ethiopian coffee samples using lignin modified glassy carbon electrode. J Anal. Methods Chem. vol. 2017, pp. 1-8. doi: 10.1155/2017/3979068.
Harnisch J.A., Gazda D. B., Anderegg J. W., Porter M. D. Chemical modification of carbonaceous stationary phases by the reduction of diazonium salts. Anal. Chem., 2001, vol. 73, no. 16, pp. 3954-3959. doi:10.1021/ac010398x.
Chamoulaud G., Bélanger D. Spontaneous derivatization of a copper electrode with in situ generated diazonium cations in aprotic and aqueous media. J. Phys. Chem. C, 2007, vol. 111, no. 20, pp. 7501-7507. doi: 10.1021/jp0704012.
Downard A. J. Potential-dependence of self-limited films formed by reduction of aryldiazonium salts at glassy carbon electrodes. Langmuir, 2000, vol. 16, no. 24, pp. 9680-9682. doi: 10.1021/la000866i.
Marcoux P. R., Hapiot P., Batail P., Pinson J. Electrochemical functionalization of nanotube films: growth of aryl chains on single-walled carbon nanotubes. New J. Chem., 2004, vol. 28, pp. 302-307. doi: 10.1039/B309509F.
Berger F., Delhalle J., Mekhalif Z. Hybrid coating on steel: ZnNi electrodeposition and surface modification with organothiols and diazonium salts. Electrochim. Acta,
vol. 53, no. 6, pp. 2852-2861. doi: 10.1016/j.electacta.2007.10.067.
Anariba F., DuVall S. H, McCreery R. L. Mono − and multilayer formation by diazonium reduction on carbon surfaces monitored with atomic force microscopy “Scratching”. Anal. Chem. 2003, vol. 75, no. 15, pp. 3837-3844. doi: 10.1021/ac034026v.
Kariuki J. K., McDermott M. T. Nucleation and growth of functionalized aryl films on graphite electrodes. Langmuir, 1999, vol. 15, no. 19, pp. 6534-6540. doi:10.1021/la990295y.
Kariuki J. K., McDermott M. T. Formation of multilayers on glassy carbon electrodes via the reduction of diazonium salts. Langmuir, 2001, vol. 17, no 19, pp. 5947-5951. doi:10.1021/la010415d.
DOI: https://doi.org/10.15826/analitika.2020.24.1.007
Ссылки
- На текущий момент ссылки отсутствуют.
