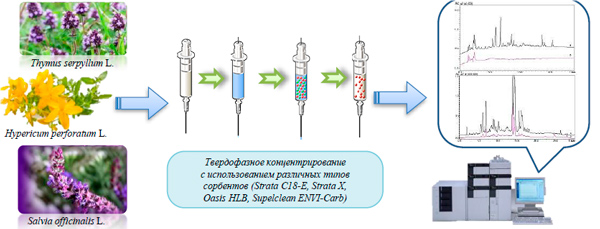
ТВЕРДОФАЗНОЕ КОНЦЕНТРИРОВАНИЕ ФЕНОЛЬНЫХ СОЕДИНЕНИЙ ИЗ ВОДНЫХ ЭКСТРАКТОВ ЛЕКАРСТВЕННЫХ РАСТЕНИЙ СЕМЕЙСТВ ЗВЕРОБОЙНЫЕ И ЯСНОТКОВЫЕ НА СОРБЕНТАХ РАЗЛИЧНОЙ ПРИРОДЫ
Аннотация
Работа посвящена твердофазному концентрированию различных типов фенольных соединений из водных экстрактов лекарственного растительного сырья семейств Зверобойные (Hypericum perforatum L.) и Яснотковые (Thymus serpyllum L., Salvia officinalis L.) с использованием различных сорбционных материалов для их дальнейшей идентификации. В качестве твердофазных сорбционных материалов использовали известные в аналитической практике октадецилсиликагель (Strata C18-E), сополимер стирола и дивинилбензола, химически модифицированный N-винилпирролидоном (Strata X), сополимер дивинилбензола и N-винилпирролидона, проявляющий гидрофильно-липофильную двойственность (Oasis HLB), а также непористый графитированный углерод (Supelclean ENVI-Carb). Для каждого из сорбентов получены основные сорбционные характеристики по отношению к целевым соединениям, а также их десорбционные параметры. Использование полимерных материалов Strata X и Oasis HLB позволяет извлекать из водных экстрактов растений целевые соединения при пяти-, а в случае с гидрофильно-липофильным сорбентом при 32- и 20-кратном концентрировании. Октадецилсиликагель показывает полноту десорбции флавоноидов (R ≥ 90 %), однако по отношению к фенолкарбоновым кислотам его использование нецелесообразно ввиду низких значений степеней извлечения аналитов (R ≤ 40 %). Достаточно универсальными сорбционными свойствами обладают гидрофильно-липофильные материалы (Oasis HLB), обеспечивающие высокие значения коэффициентов концентрирования при приемлемых значениях степеней извлечения фенолкарбоновых кислот (R ≤ 96 %) и флавоноидов (R ≤ 91 %). Сорбция фитокомпонентов непористым углеродным сорбентом Supelclean ENVI-Carb дает достаточно высокие характеристики, но процесс десорбции данных соединений затруднителен и требует дальнейшего изучения. Использование различных типов сорбентов показывает, что минорные компоненты, которые не детектируются в обычных условиях их хроматографического определения, могут быть сконцентрированы ТФЭ для дальнейшей их идентификации, что обеспечит расширение круга определяемых соединений в составе различных лекарственных растений. Предложенная схема ТФЭ фенольных компонентов может быть в дальнейшем использована для анализа растительных материалов других семейств.
Ключевые слова: зверобой, чабрец, шалфей, твердофазная экстракция, флавоноиды, фенольные кислоты, лекарственное растительное сырье
DOI: http://dx.doi.org/10.15826/analitika.2020.24.2.002Полный текст:
PDF (Russian)Литература
REFERENCES
Moleriu L., Jianu C., Bujanca G., Doros G., Misca C., Ilie O., Moleriu R., Ilie A. Essential Oil of Hypericum perforatum. The chemical composition and antimicrobial activity. Revista de Chimie, 2017, vol. 68, pp. 687-692. doi: 10.37358/RC.17.4.5531
Greeson J., Sanford B., Monti D. St. John’s wort (Hypericum perforatum): a review of the current pharmacological, toxicological, and clinical literature. Psychopharmacology, 2001, vol. 153. no. 4, pp. 402–414. doi: 10.1007/s002130000625
Khoddami A., Wilkes M., Roberts T. Techniques for Analysis of Plant Phenolic Compounds. Molecules, 2013, vol. 18, no. 2, pp. 2328–2375. doi: 10.3390/molecules18022328
Romanik G., Gilgenast E., Przyjazny A., Kaminski M. Techniques of preparing plant material for chromatographic separation and analysis. Journal of Biochemical and Biophysical Methods, 2007, vol. 70, no. 2, pp. 253–261. doi: 10.1016/j.jbbm.2006.09.012
Robards K. Strategies for the determination of bioactive phenols in plants, fruit and vegetables. Journal of Chromatography A, 2003, vol. 1000, no. 1-2, pp. 657–691. doi: 10.1016/S0021-9673(03)00058-X
De Rijke E., Out P., Niessen W. M. A., Ariese F., Gooijer C., Brinkman U. A. T. Analytical separation and detection methods for flavonoids. Journal of Chromatography A, 2006, vol. 1112, no. 1-2, pp. 31–63. doi: 10.1016/j.chroma.2006.01.019
Olejnic E. Ju., Blinova I. P., Dejneka L. A., Kul'chenko Ja. Ju., Dejneka V. I., Selemenev V. F. [Anthocyanins and other phenolic compounds of Ivan-tea drink and its antioxidant activity]. Vestnik VGU, seriia: Khmiia. Biologiia. Farmatsiia [Proceedings of Voronezh State University. Series: Chemistry. Biology. Pharmacy], 2018, no. 1, pp. 7-14 (in Russian).
Del Alamo M., Casado L., Hernandez V., Jimenez J. J. Determination of free molecular phenolics and catechins in wine by solid phase extraction on polymeric cartridges and liquid chromatography with diode array detection. Journal of Chromatography A, 2004, vol. 1049, no. 1-2, pp. 97–105. doi: 10.1016/j.chroma.2004.08.017
Sun C., Tan H., Zhang Y., Zhang H. Phenolics and abscisic acid identified in acacia honey comparing different SPE cartridges coupled with HPLC-PDA. Journal of Food Composition and Analysis, 2016, vol. 53, pp. 91–101. doi: 10.1016/j.jfca.2016.08.006
Andrade-Eiroa A., Canle M., Leroy-Cancellieri V., Cerda, V. Solid-phase extraction of organic compounds: A critical review (Part I). Trends in Analytical Chemistry, 2016, vol. 80, pp. 641–654. doi: 10.1016/j.trac.2015.08.015
Magiera S., Zaręba M. Chromatographic Determination of Phenolic Acids and Flavonoids in Lycium barbarum L. and Evaluation of Antioxidant Activity. Food Analytical Methods, 2015, vol. 8, no. 10, pp. 2665–2674. doi:10.1007/s12161-015-0166-y
Cobzac S., Gocan S. Sample preparation for high performance liquid chromatography: recent progress. Journal of Liquid Chromatography & Related Technologies, 2011, vol.3 4, no. 13, pp. 1157-1267. doi: 10.1080/10826076.2011.588064
Kozyra M, Glowniak K. Phenolic acids in extracts obtained from the flowering herbs of Cirsium vulgare (Savi) Ten. growing in Poland. Acta Societatis Botanicorum Poloniae, 2013, vol. 82, pp. 325-329. doi: 10.5586/asbp.2013.039
Zgorka G., Glowniak K. Variation of free phenolic acids in medicinal plants belonging to the Lamiaceae family. Journal of Pharmaceutical and Biomedical Analysis, 2001, vol. 26, no. 1, pp. 79-87. doi: 10.1016/S0731-7085(01)00354-5
Simplified Solid Phase Extraction Solutions. Available at: http:// www.phenomenex.com. (accessed 28 October 2019).
Trakunram K., Janchawee B., Raungrut P., Prutipanlai S. Solid-phase extraction for determination of caffeine and its dimethylxanthine metabolites in rat urine using high performance liquid chromatography and its application. Songklanakarin Journal of Science and Technology, 2018, vol. 40, no. 4, pp. 759-766. doi:10.14456/sjst-psu.2018.116
Fontanals N., Marce R., Borrull F. Materials for Solid-Phase Extraction of Organic Compounds. Separations, 2019, vol. 6, no. 4-56, pp. 1-27. doi: 10.3390/separations6040056
Cserhati T. Carbon-based sorbents in chromatography. New achievements. Biomedical Chromatography, 2009, vol. 23, no. 2, pp. 111–118. doi:10.1002/bmc.1168
ALOthman Z. A., Wabaidur S. M. Application of carbon nanotubes in extraction and chromatographic analysis: A review. Arabian Journal of Chemistry, 2019, vol. 12, no. 5, pp. 633-651. doi: 10.1016/j.arabjc.2018.05.012
Ziyatdinova G., Kozlova E., Budnikov H. Poly(gallic acid)/MWNT-modified electrode for the selective and sensitive voltammetric determination of quercetin in medicinal herbs. Journal of Electroanalytical Chemistry, 2018, vol. 821, pp. 73–81. doi: 10.1016/j.jelechem.2017.12.071
Palma M., Pineiro Z., Barroso C.G. In-line pressurized-fluid extraction-solid-phase extraction for determining phenolic compounds in grapes. Journal of Chromatography A, 2002, vol. 968, no. 1-2, pp. 1-6. doi: 10.1016/s0021-9673(02)00823-3
FS.2.5.0015.15. Gosudarstvennaia Farmakopeia Rossiiskoi Federatsii [State Pharmacopoeia of the Russian Federation]. Moscow, 2018, Issue 14, vol. 4, pp. 6074-6083 (in Russian)
Milevskaya V.V., Statkus M.A., Temerdashev Z. A, Kiseleva N.V., Butyl’skaya T.S., Shil’ko E.A. Extraction and Determination of Biologically Active Components of St. John’s Wort and Its Pharmaceutical Preparations. Journal of Analytical Chemistry, 2016, vol.71, no.7, pp.741-747. doi: 10.7868/S0044450216070136
Bielicka-Daszkiewicz K., Voelkel A. Theoretical and experimental methods of determination of the breakthrough volume of SPE sorbents. Talanta, 2009, vol. 80, no. 2, pp. 614-621. doi: 10.1016/j.talanta.2009.07.037
Sychev K.S., Davankov V.A. [Materials and methods for sample preparation in chromatography: solid-phase concentration and adsorption]. Sorbtsionnye i khromatograficheskie protsessy [Sorption and chromatographic processes], 2004, vol. 4, no. 1, pp. 5-28 (in Russian)
Ajila C., Brar S., Verma M., Tyagi M., Godbout S., Valero J. Extraction and Analysis of Polyphenols: Recent trends. Critical Reviews in Biotechnology, 2011, vol. 31, no. 3, pp. 227-249. doi: 10.3109/07388551.2010.513677
Shil’ko E.A., Milevskaya V.V., Temerdashev Z. A., Kiseleva N.V. [Sorption characteristics of sorbents for solid-phase extraction of phenolic compounds from extracts of medicinal plants]. Sorbtsionnye i khromatograficheskie protsessy [Sorption and chromatographic processes], 2019, vol. 19, no. 2, pp. 157-167. doi: 10.17308/sorpchrom.2019.19/733 (in Russian)
Shil’ko E.A., Milevskaya V.V., Temerdashev Z. A., Kiseleva N.V. [Solid phase concentration of phenolic compounds from the aqueous medicinal raw plant material extracts on the example of St. John’s Wort (Hypericum perforatum L.)]. Analitika i kontrol’ [Analytics and Control], 2018, vol. 22, no. 3, pp. 303-314. doi: 10.15826/analitika.2018.22.3.013 (in Russian)
DOI: https://doi.org/10.15826/analitika.2020.24.2.002
Ссылки
- На текущий момент ссылки отсутствуют.
